Каковы преимущества использования катализаторов в промышленности?
Химическая реакция - это процесс, в ходе которого атомы реактивов собираются вместе и объединяются или перестраиваются для образования продуктов. Примером химической реакции может служить реакция газа азота и водорода на производство аммиака:
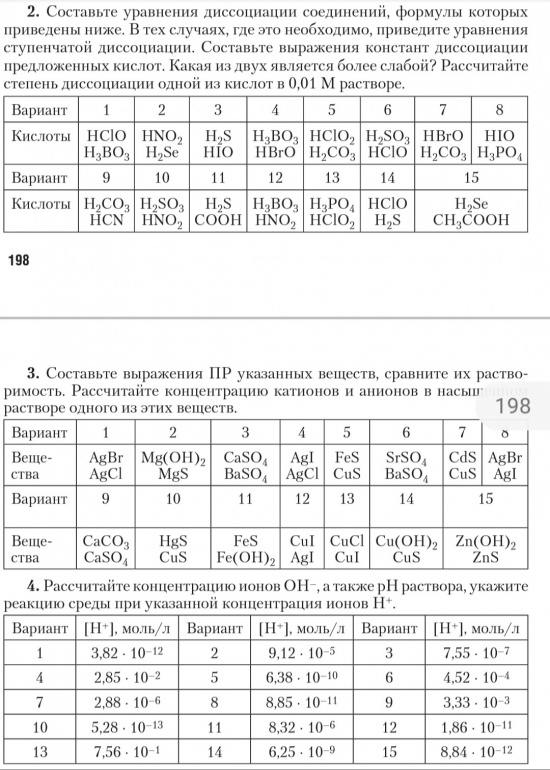
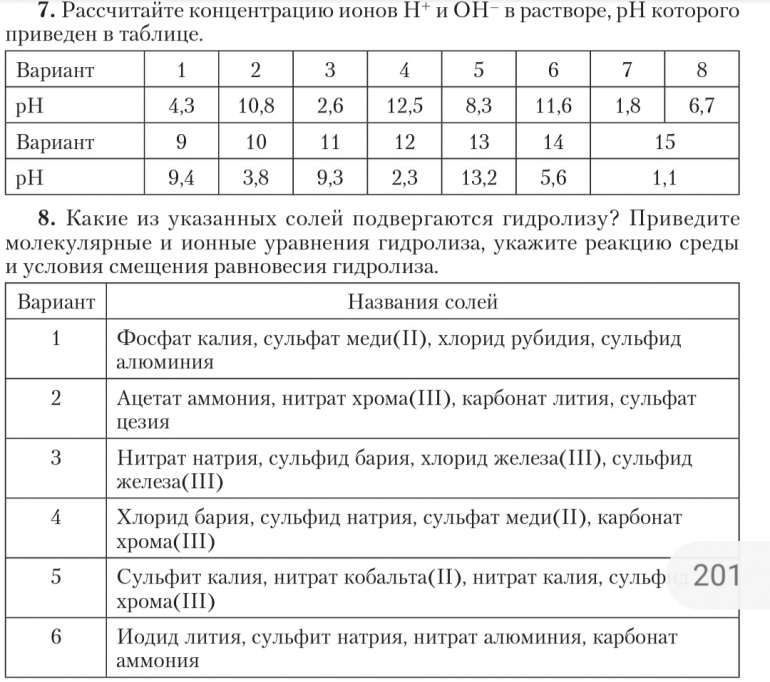
N_2 + 3H_2 -> 2NH_3 . Это пример первого, где сочетаются атомы. Примером последнего является окисление метана с образованием двуокиси углерода и воды.
Для осуществления химических реакций необходимо учитывать ряд факторов. Например, реактивы должны собираться вместе - сталкиваться. Столкновение также должно происходить с реактивами, имеющими определенную ориентацию, и столкновение должно происходить с реактивами, обладающими достаточным количеством энергии. Все эти факторы способствуют образованию энергетического барьера химических реакций, известного как энергия активации. Различные химические реакции имеют разную энергию активации, и более высокие энергии активации означают, что реакция будет протекать медленнее, или вообще не протекать при определенных условиях.
В промышленной среде реакция с высокой энергией активации не является привлекательной инвестицией, поскольку крупномасштабное производство будет сдерживаться затратами и временем, связанными с химической реакцией, обладающей высокой энергией активации. Выходом из сложившейся ситуации является использование катализаторов.
Катализаторы - это молекулы, которые снижают энергию активации химической реакции без фактического участия в ней. Они делают это, предоставляя альтернативный путь к реакции. Примером биологических катализаторов являются ферменты. Например, при синтезе белка ферменты отвечают за присоединение определенной аминокислоты в цепочку - таким образом, это иллюстрирует функцию катализаторов как видов, которые обеспечивают правильную ориентацию реагирующих видов (и со специфичностью).
В промышленности катализаторы позволят снизить себестоимость производства, а также сократить время производства некоторых видов химических веществ, что сделает производство максимально эффективным. В качестве примера можно привести использование железных или платиновых поверхностей для каталитического производства аммиака в результате реакции водорода и азота (см. выше). Эта реакция является очень неэффективной и дорогостоящей без использования катализаторов.
Существуют и другие катализаторы - некоторые специфические, некоторые общеприменимые - используемые в промышленности, включая оксид ванадия для производства серной кислоты, алюмосиликаты для преобразования эфира в этанол, цеолиты для каталитического крекинга масел и другие.
Все эти катализаторы снижают энергию активации реакции, обеспечивая альтернативный путь к конечному продукту и, следовательно, повышают эффективность реакции. В промышленной среде это позволит сократить время и, в конечном счете, стоимость производства продукта.

Другие вопросы в разделе - Химия

Объясните, как функционирует мыло, ссылаясь на его фосфолипидные свойства. ...

Приведите пример, описывающий взаимосвязь между дистилляцией и хроматографией. ...





 ...
...